КонсультантПлюс: примечание.
Нумерация пунктов дана в соответствии с официальным текстом документа.
- Отсутствием специфических диагностических критериев, сходство клинических проявлений сердечно-сосудистой и дыхательной недостаточности, особенно на фоне генерализованной инфекционной патологии затрудняет диагностику миокардитов. Ранняя манифестации (в том числе у новорожденных) различных форм врожденных кардиомиопатий, заболеваний миокарда неизвестной этиологии (включая эндомиокардиальный фиброэластоз), в генезе которых наряду с другими факторами большое значение придается инфекции в раннем фетальном периоде.
- При дифдиагностике с идиопатической дилатационной кардиомиопатией (ДКМП) решающее значение имеет постепенное развитие симптомов застойной сердечной недостаточности, отсутствие или минимальные лабораторные признаки воспаления, отсутствие эффекта от противовоспалительной терапии. Несмотря на существующие критерии диагностики миокардитов и кардиомиопатий (заболеваний миокарда неизвестной этиологии, по определению ВОЗ), дифференциальная диагностика этих состояний, особенно у детей первого года жизни, очень сложна, так как между ними существует не только клиническое и патогенетическое, но и морфологическое сходство, общность электрокардиографических и эхокардиографических характеристик. Эндомиокардиальная биопсия миокарда, показанная в этих случаях, часто (но не всегда) подтверждает диагноз.
- Дифференциальная диагностика ревматических и неревматических миокардитов основана на исключении ревматической лихорадки, наблюдающейся у детей старше 5 - 7 лет. Характерны наличие связи манифестации миокардита с перенесенной стрептококковой инфекцией, имеют место экстракардиальные проявления - анулярная сыпь, артралгии, полиартрит, хорея. Для ревматического миокардита не характерна кардиомегалия и выраженная миокардиальная недостаточность, часто в процесс вовлекается перикард, рано может обнаруживаться деформация атриовентрикулярных клапанов, в дальнейшем формируются пороки сердца. Обнаруживаются лабораторные изменения, типичные для острой ревматической лихорадки (лейкоцитоз, повышение СОЭ, высокие титры АСЛО, CRP, антиген 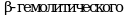 стрептококка группы A), при бактериологическом исследовании мазка из зева может выделяться
стрептококка группы A), при бактериологическом исследовании мазка из зева может выделяться 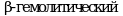 стрептококк группы A. Характерны: отчетливая устойчивая положительная динамика признаков декомпенсации кровообращения, изменений ЭКГ, ликвидация перикардиального выпота на фоне противовоспалительной и антибиотикотерапии.
стрептококк группы A. Характерны: отчетливая устойчивая положительная динамика признаков декомпенсации кровообращения, изменений ЭКГ, ликвидация перикардиального выпота на фоне противовоспалительной и антибиотикотерапии.
- Миокардиты новорожденных с кардиомегалией, цианозом, тахикардией, декомпенсацией кровообращения достаточно сложно дифференцировать с другими кардиомегалиями новорожденных, хотя это важно для назначения адекватной терапии и определения прогноза заболевания. В генезе различных форм врожденных кардиомиопатий и эндомиокардиального фиброэластоза наряду с другими факторами большое значение придается инфекции в раннем фетальном периоде. Любое интеркуррентное заболевание у ребенка грудного возраста может стать триггером манифестации этих врожденных заболеваний.
- Эндомиокардиальный фиброэластоз (ФЭ) - врожденное заболевание неясной этиологии, начинающееся во внутриутробном периоде, характеризующееся значительным утолщением эндокарда, обусловленным фиброзом, кардиомегалией и застойной сердечной недостаточностью. Считается, что фиброэластоз не является самостоятельным заболеванием, а представляет собой неспецифическую реакцию эндокарда на любой миокардиальный стресс, в качестве которого могут выступать гемодинамические перегрузки из-за врожденных пороков сердца и сосудов и их сочетаний, вирусные или бактериальные агенты, генетические аберрации, гипоксия, кардиомиопатии и т.д. Клинические проявления варьируют. На первом плане стоят кардиомегалия и рано появляющаяся декомпенсация кровообращения у новорожденных, чаще - у детей грудного возраста (до 6 месяцев). Признаки тяжелой застойной недостаточности могут развиваться у ранее клинически здорового ребенка, манифестация и прогрессирование может обнаруживаться на фоне рецидивирующих легочных инфекций. Симптомы заболевания могут носить постоянно прогрессирующий характер или протекать с периодами ремиссии. Прогноз неблагоприятен.
- Неинфекционные кардиомегалии новорожденных - представлены острыми цереброкардиальным и кардиопульмональным синдромами, афоничными врожденными пороками сердца и гетерогенной группой генетических и врожденных заболеваний (гликогенозная кардиомегалия - болезнь Помпе или гликогеноз II типа, митохондриальная патология, врожденные миопатии и прогрессирующие мышечные дистрофии), эти заболевания характеризуются плохим прогнозом.
- Транзиторная ишемия миокарда новорожденных (постгипоксический синдром дезадаптации сердечно-сосудистой системы, цереброкардиальный синдром) развивается на фоне неврологических эквивалентов перенесенной гипоксии, кардиопульмональный синдром или острое легочное сердце (cor pulmonalis acutum) при респираторном дистресс-синдроме, при множественных ателектазах в возрасте нескольких дней.
- К врожденным порокам сердца (ВПС) и сосудов с кардиомегалией, но без выраженной аускультативной симптоматики, относятся аномальное отхождение левой коронарной артерии от легочной артерии, синдром Бланда-Уайта-Гарланда (Bland-White-Garland), изолированная коарктация аорты, полная форма общего открытого атриовентрикулярного канала, дефект межпредсердной перегородки, тотальный или частичный аномальный дренаж легочных вен. Возможна кардиомегалия, связанная с аритмогенной кардиопатией при фетальных аритмиях. Основным в исключении всех видов афоничных ВПС является Эхо-КГ исследование, также необходимы пульсоксиметрия на верхних и нижних конечностях у новорожденных (для диагностики коарктации аорты и других дуктус-зависимых пороков), информативны электрокардиографические исследования (для синдрома Бланда-Уайта-Гарленда).
- Аритмогенная дисфункция миокарда с признаками недостаточности миокарда и дилатацией камер сердца развивается у 15 - 80% больных с хроническими тахиаритмиями (эктопической предсердной тахикардией, предсердножелудочковой тахикардией, желудочковой тахикардией, хронической формой трепетания предсердий). Более высокий риск развития аритмогенной дисфункции миокарда наблюдается при стабильно высокой частоте сердечного ритма в течение суток.
- Степень дисфункции варьирует от умеренной дилатации ЛЖ до значительного расширения камер сердца по типу синдрома дилатационной кардиомиопатии с резким снижением сократимости миокарда, выраженными признаками хронической сердечной недостаточности. Рентгенологическая картина неспецифична. Отсутствие явной связи с перенесенной инфекцией, нормальные значения или умеренное повышение уровня биохимических маркеров повреждения миокарда, постепенное, но довольно быстрое (2 - 4 недели) повышение фракции выброса и нормализация полостей сердца после устранения аритмии подтверждают предположение об аритмогенном генезе кардиомегалии и дисфункции миокарда.
- Легкие формы миокардита у детей школьного возраста и подростков следует дифференцировать с миокардиодистрофией на фоне вегетативной дисфункции, особенно при наличии наджелудочковой экстрасистолии, кардиалгического синдрома. Главным отличием является отсутствие кардиомегалии и сердечной недостаточности, отсутствие повышения уровня биохимических маркеров повреждения миокарда, наличие ярких вегетативных нарушений со стороны других органов и систем. ЭКГ-изменения, как правило, исчезают на фоне физической нагрузки (в отличие от миокардита).
- Гражданский кодекс (ГК РФ)
- Жилищный кодекс (ЖК РФ)
- Налоговый кодекс (НК РФ)
- Трудовой кодекс (ТК РФ)
- Уголовный кодекс (УК РФ)
- Бюджетный кодекс (БК РФ)
- Арбитражный процессуальный кодекс
- Конституция РФ
- Земельный кодекс (ЗК РФ)
- Лесной кодекс (ЛК РФ)
- Семейный кодекс (СК РФ)
- Уголовно-исполнительный кодекс
- Уголовно-процессуальный кодекс
- Производственный календарь на 2025 год
- МРОТ 2026
- ФЗ «О банкротстве»
- О защите прав потребителей (ЗОЗПП)
- Об исполнительном производстве
- О персональных данных
- О налогах на имущество физических лиц
- О средствах массовой информации
- Производственный календарь на 2026 год
- Федеральный закон "О полиции" N 3-ФЗ
- Расходы организации ПБУ 10/99
- Минимальный размер оплаты труда (МРОТ)
- Календарь бухгалтера на 2026 год
- Частичная мобилизация: обзор новостей
- Постановление Правительства РФ N 1875